Đề bài
Kết quả phân tích nguyên tố cho thấy trong hợp chất X: carbon chiếm 61,02%; hydrogen chiếm 15,25 %; còn lại là nitrogen về khối lượng. Từ phổ khối lượng của X xác định được giá trị m / z của peak [M+] bằng 59.
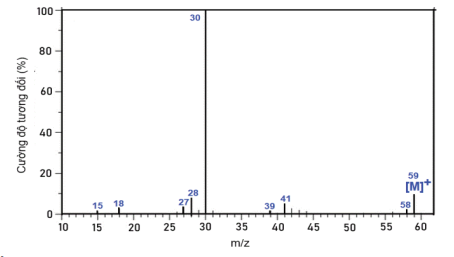
X có thể là chất nào sau đây:
$\left( \text{CH}_{3} \right)_{3}\text{N}$.
$\text{CH}_{3}\text{NH}_{2}$.
$\text{C}_{3}\text{H}_{7}\text{N}$.
$\text{C}_{2}\text{H}_{7}\text{N}$.
Phương pháp giải
Xác định công thức đơn giản nhất của chất X theo tỉ lệ phần trăm các nguyên tố.
Từ phổ khối, biết được phân tử khối của X.
Từ đó, xác định được công thức phân tử của X.
Lời giải chi tiết
Phần trăm nitrogen về khối lượng là: $%N=100%-61,02%-15,25%=23,73%$.
Gọi công thức hoá học của X là ${{C}_{\text{x}}}{{H}_{y}}{{N}_{\text{z}}}$.
Ta có:
$x:y:z=\frac{61,02%}{12}:\frac{15,25%}{1}:\frac{23,73%}{14}=3:9:1$
Công thức đơn giản nhất của X là: ${{C}_{3}}{{H}_{9}}N$
Mà theo phổ khối, khối lượng phân tử X là 59.
Do đó, công thức phân tử của X là: ${{C}_{3}}{{H}_{9}}N$ hay ${{(C{{H}_{3}})}_{3}}N$
Lời giải chi tiết
Phân tích đề bài:
Đề bài cho biết thành phần phần trăm khối lượng các nguyên tố trong X:
- Carbon (C) chiếm 61,02%
- Hydrogen (H) chiếm 15,25%
- Nitrogen (N) chiếm 23,73% (do còn lại là nitrogen: 100% - 61,02% - 15,25%)
Xác định công thức phân tử dựa theo giá trị m/z của peak [M+] bằng 59.
Phân tích các phương án:
Ta cần kiểm tra các công thức có thể phù hợp với cả thành phần phần trăm khối lượng và m/z bằng 59:
- A. $\left( \text{CH}_{3} \right)_{3}~\text{N}$:
- Khối lượng mol: $3 \times 12{,}01 + 9 \times 1{,}008 + 14{,}01 = 59{,}11$ g/mol
- Tỷ lệ C: \( \frac{3 \times 12{,}01}{59{,}11} \times 100\% = 61{,}02\% \)
- Tỷ lệ H: \( \frac{9 \times 1{,}008}{59{,}11} \times 100\% = 15{,}36\% \)
Khối lượng mol phù hợp với m/z và tỷ lệ khối lượng các nguyên tố. - B. $\text{CH}_{3}\text{NH}_{2}$:
- Khối lượng mol: $12{,}01 + 5 \times 1{,}008 + 14{,}01 = 31{,}07$ g/mol
Không phù hợp với m/z = 59. - C. $\text{C}_{3}\text{H}_{7}~\text{N}$:
- Khối lượng mol: $3 \times 12{,}01 + 7 \times 1{,}008 + 14{,}01 = 57{,}11$ g/mol
Khối lượng gần 59 nhưng không khớp. - D. $\text{C}_{2}\text{H}_{7}~\text{N}$:
- Khối lượng mol: $2 \times 12{,}01 + 7 \times 1{,}008 + 14{,}01 = 45{,}09$ g/mol
Không phù hợp với m/z = 59.
Kết luận: Chọn A. $\left( \text{CH}_{3} \right)_{3}~\text{N}$. Công thức này tương ứng với khối lượng mol 59 và tỷ lệ phần trăm khối lượng các nguyên tố.
Chú ý khi giải
Lưu ý khi giải:
- Xác định chính xác khối lượng phân tử dựa vào phổ khối lượng (m/z).
- Tính tỷ lệ phần trăm khối lượng các nguyên tố để kiểm tra sự phù hợp với lựa chọn.
- Chú ý các trường hợp có khối lượng gần giống nhưng không khớp hoàn toàn với m/z đã cho.