Đề bài
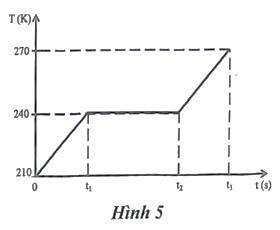
Để tìm hiểu về các quá trình chuyển thể của ammonia (NH), người ta đun nóng 500 gam ammonia lỏng ở nhiệt độ 210 K trong một cốc chịu nhiệt dưới áp suất chuẩn (1 atm). Biết rằng năng lượng nhiệt được cung cấp không đều đặn. Cho nhiệt dung riêng, nhiệt nóng chảy riêng và nhiệt hóa hơi riêng của ammonia lần lượt là C = 4 710 JkgK, L=1,37.106 J/kg. Theo dõi sự thay đổi nhiệt độ của ammonia theo thời gian, người ta thu được đồ thị như Hình 5.
Lời giải chi tiết
Đề bài gồm 4 mệnh đề và yêu cầu xác định tính đúng sai của các mệnh đề đó. Ta phân tích từng mệnh đề như sau:
Mệnh đề 1
Nhiệt độ sôi của ammonia là 513 °C.
Ta cần kiểm tra nhiệt độ sôi tiêu chuẩn của ammonia trong các tài liệu khoa học. Nhiệt độ sôi của NH3 là khoảng -33,34 °C, không phải 513 °C. Do đó, mệnh đề này sai.
Mệnh đề 2
Cần cung cấp 685 kJ nhiệt lượng để 500 g ammonia hóa hơi hoàn toàn ở nhiệt độ sôi của nó.
Tính nhiệt lượng cần thiết để hóa hơi 500 g (0.5 kg) ammonia:
\[ Q = m \times L = 0.5 \times 1.37 \times 10^6 = 685,000 \text{ J} = 685 \text{ kJ} \]Kết quả này trùng khớp với mệnh đề, do đó mệnh đề 2 là đúng.
Mệnh đề 3
Từ thời điểm t1 đến thời điểm t2, thế năng tương tác của các phân tử ammonia tăng nhưng động năng tịnh tiến trung bình của chúng không thay đổi.
Từ thời điểm t1 đến t2 nhiệt độ không đổi, do đó thế năng tăng (do chuyển pha), trong khi động năng tịnh tiến trung bình không thay đổi. Mệnh đề này là đúng.
Mệnh đề 4
Tổng nhiệt lượng cần cung cấp cho lượng ammonia kể từ khi bắt đầu đun đến thời điểm t2 lớn hơn 760 kJ.
Tính tổng nhiệt lượng:
1. Từ 210 K lên 240 K:
\[ Q_1 = m \times C \times \Delta T = 0.5 \times 4710 \times (240 - 210) = 70,650 \text{ J} \]2. Để chuyển pha từ lỏng thành hơi ở cùng nhiệt độ:
\[ Q_2 = 685,000 \text{ J} \]Tổng:
\[ Q_{total} = Q_1 + Q_2 = 70,650 + 685,000 = 755,650 \text{ J} \approx 756 \text{ kJ} \]Mệnh đề 4 là sai vì tổng nhiệt lượng cần cung cấp là 756 kJ, nhỏ hơn 760 kJ.
Chú ý khi giải
- Cần nắm vững công thức tính nhiệt lượng cho các quá trình chuyển thể.
- Tìm hiểu và ghi nhớ các thông số nhiệt độ sôi, nhiệt nóng chảy, nhiệt hóa hơi của chất cụ thể từ tài liệu đáng tin cậy.
- Luôn chuyển đổi đơn vị khối lượng và năng lượng để đảm bảo tính toán chính xác.