Đề bài
Phương trình hóa học của phản ứng giữa acetic acid với ethyl alcohol thu được ethyl acetate là:
$\text{CH}_{3}\text{COOH} + \text{C}_{2}\text{H}_{5}\text{OH}\underset{~}{\overset{t^{0};\,\,\,\text{H}_{2}\text{SO}_{4}ñaëc}{\rightleftharpoons}\ }\text{CH}_{3}\text{COOC}_{2}\text{H}_{5} + \text{H}_{2}\text{O}$
Ion H⁺ tham gia giai đoạn (1) trong cơ chế của phản ứng trên như sau:
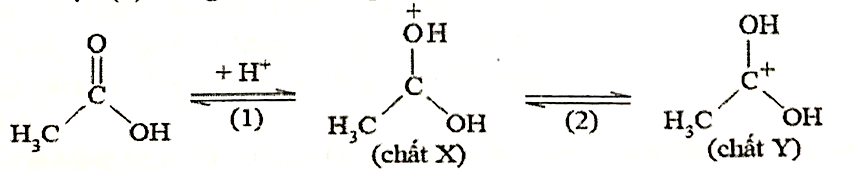
Cho các phát biểu sau:
(a) Trong giai đoạn (1) có sự phân cắt liên kết π.
(b) Chất X và Y kém bền vì mỗi chất đều chứa một nguyên tử chưa đạt cấu hình của khí hiếm.
(c) Trong giai đoạn (1), ion H⁺ nhận hai cặp electron chưa liên kết của nguyên tử oxygen trong acetic acid.
(d) Nếu thay xúc tác $H_{2}SO_{4}$ đặc bằng $H_{2}SO_{4}$ loãng thì hiệu suất phản ứng không thay đổi vì cân bằng đều chuyển dịch theo chiều thuận.
Các phát biểu đúng là
(b), (c), (d).
(a), (b).
(b), (c).
(a), (b), (d).
Phương pháp giải
Dựa vào cơ chế phản ứng giữa acetic acid với ethyl alcohol thu được ethyl acetate.
Lời giải chi tiết
Phân tích các phát biểu:
(a) Đúng, vì giai đoạn (1) của phản ứng xảy ra sự phân cắt liên kết π ở C=O.
(b) Đúng, vì chất X và Y là trung gian có chứa các ion dương, làm cho chúng kém bền.
(c) Sai, vì trong giai đoạn này, ion H⁺ chỉ nhận một cặp electron chưa liên kết để hình thành liên kết mới với oxygen.
(d) Sai, vì việc thay thế $H_{2}SO_{4}$ đặc bằng $H_{2}SO_{4}$ loãng sẽ làm giảm nồng độ H⁺, do đó hiệu suất phản ứng sẽ giảm chứ không giữ nguyên.