Đề bài
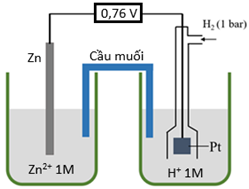
Cho pin điện hóa được thiết lập bởi điện cực Zn và điện cực hydrogen (cấu tạo như hình vẽ) dung dịch Zn (aq) 1 M và dung dịch $H^{+}$ (aq) 1 M có thể tích bằng nhau, sức điện động chuẩn của pin đo được là 0,76 V.
Phương pháp giải
Dựa vào phương trình hóa học xảy ra trong pin.
Lời giải chi tiết
1) Sai, vì $E_{pin}^{o} = E_{2H^{+}/H_{2}}^{o} - E_{Zn^{2 +}/Zn}^{o} = 0,76(V)$
Mà $E_{2H^{+}/H_{2}}^{o} = 0(V)$ nên $E_{Zn^{2 +}/Zn}^{o} = - 0,76(V)$
2) Đúng, vì $\left. Zn(s) + 2H^{+}(aq)\rightarrow H_{2}(g) + Zn^{2 +}(aq) \right.$nên nồng độ $Zn^{2 +}$ tăng 0,1M thì nồng độ $H^{+}$ giảm 0,2M (còn 0,8M).
3) Đúng, vì tại cực dương (cathode) xảy ra bán phản ứng: $\left. 2H^{+} + 2e\rightarrow H_{2} \right.$
4) Sai, vì $E_{2H^{+}/H_{2}}^{o} > E_{Zn^{2 +}/Zn}^{o}$ nên phản ứng xảy ra là $\left. Zn(s) + 2H^{+}(aq)\rightarrow H_{2}(g) + Zn^{2 +}(aq) \right.$