Đề bài
Tiến hành thí nghiệm như sơ đồ dưới đây:
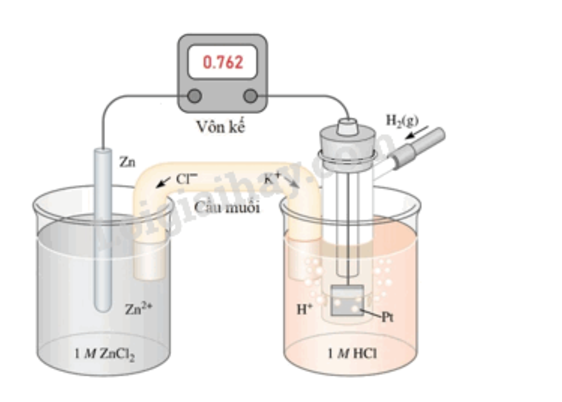
Cho thanh kẽm vào dung dịch $ZnCl_{2}$ 1 M. Nối thanh kẽm với điện cực hydrogen tiêu chuẩn thông qua vôn kế (voltmeter). Điện áp đo được là 0,762V.
Phát biểu nào sau đây về thí nghiệm trên không đúng?
Zn là cực âm (anode) và điện cực hydrogen tiêu chuẩn là cực dương (cathode).
Tại cực âm, Zn nhường electron và tại cực dương, ion $H^{+}$ nhận electron thành khí $H_{2}$.
Nếu quy ước thế điện cực chuẩn của hydrogen bằng 0 V thì thế điện cực chuẩn của cặp $Zn^{2 +}/Zn$ là +0,762 V.
Phương trình hóa học của phản ứng xảy ra trong pin là: $\left. Zn(s) + 2H^{+}\left( {aq} \right)\rightarrow Zn^{2 +}\left( {aq} \right) + H_{2}(g). \right.$
Phương pháp giải
Phân tích thí nghiệm xảy ra để rút ra nhận xét.
Lời giải chi tiết
Phân tích:
- Trong thí nghiệm, thanh kẽm (Zn) tiếp xúc với dung dịch $ZnCl_2$ 1 M và điện cực hydrogen tiêu chuẩn (SHE) tiếp xúc với dung dịch HCl 1 M. Kết nối này tạo thành một pin điện hóa.
- Điện áp đo được là 0,762 V, cho biết sự chênh lệch thế điện giữa hai điện cực.
- Các phản ứng điện cực xảy ra:
- Tại cực âm (anode): Zn nhường electron:
\[ \text{Zn}(s) \rightarrow \text{Zn}^{2+}(aq) + 2e^- \] - Tại cực dương (cathode): H+ nhận electron tạo thành khí H2:
\[ 2\text{H}^+(aq) + 2e^- \rightarrow \text{H}_2(g) \] - Phản ứng tổng quát:
\[ \text{Zn}(s) + 2\text{H}^+(aq) \rightarrow \text{Zn}^{2+}(aq) + \text{H}_2(g) \]
Phân tích các đáp án:
- A. Đúng. Zn là cực âm (anode) và điện cực hydrogen tiêu chuẩn là cực dương (cathode).
- B. Đúng. Tại cực âm, Zn nhường electron và tại cực dương, ion H+ nhận electron thành khí H2.
- C. Sai. Thế điện cực chuẩn của cặp $Zn^{2+}/Zn$ là -0,762 V, không phải +0,762 V, khi quy ước thế điện cực chuẩn của hydrogen là 0 V.
- D. Đúng. Phương trình hóa học của phản ứng xảy ra trong pin đã nêu rõ ràng.
Vì vậy, phát biểu không đúng là C.