Đề bài
Trinitroglycerol (TNG) đã được Alfred Nobel sử dụng làm chất nổ thương mại, là hợp chất nguy hiểm. TNG được sản xuất từ glycerol theo sơ đồ sau:
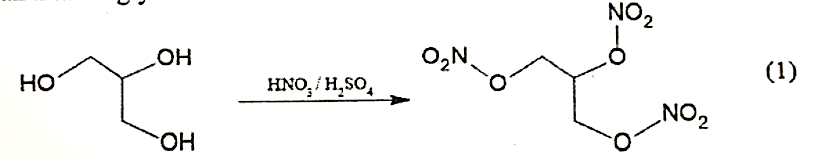
Khi nổ, TNG phân hủy theo sơ đồ: $\text{C}_{3}\text{H}_{5}\left( \text{ONO}_{2} \right)_{3}(~\text{s})\overset{\text{t}^{{^\circ}}}{\rightarrow}\text{CO}_{2}(~\text{g}) + \text{N}_{2}(~\text{g}) + \text{O}_{2}(~\text{g}) + \text{H}_{2}\text{O}(\text{g})$ (2)
Phương pháp giải
Dựa vào phản ứng sản xuất TNG từ glycerol.
Lời giải chi tiết
(1) Sai,
Phản ứng phân hủy của trinitroglycerol (TNG) là: $\text{C}_{3}\text{H}_{5}(\text{ONO}_{2})_{3}(\text{s})\rightarrow 3\text{CO}_{2}(\text{g}) + \text{1.5N}_{2}(\text{g}) + 0.25\text{O}_{2}(\text{g}) + 2.5\text{H}_{2}\text{O}(\text{g})$
- Từ đó, tính nhiệt phân hủy 1 mol TNG ($\Delta H^\circ_{\text{reaction}}$): $\Delta H^\circ_{\text{reaction}} = 3(-393.5) + 2.5(-241.8) - (-370.15) = -1261.5 - 604.5 + 370.15 = -1495.85\, \text{kJ/mol}$
Số mol TNG ứng với 227kg TNG là: ${{n}_{TNG}}=\frac{227.1000}{227}=1000mol$
Vâỵ nhiệt để phân huỷ 227kg TNG là: $1495,85.1000=14958500kJ$.
(2) Đúng, TNG có công thức: $\text{C}_{3}\text{H}_{5}(\text{ONO}_{2})_{3}$.
Do đó TNG có 3 liên kết $\pi$ trong phân tử.
(3) Đúng. Glycerol phản ứng với HNO₃ tạo 3-Nitroglycerin, có thể có nhiều đồng phân cấu tạo tùy theo vị trí nitrate hóa. Nếu phản ứng theo tỉ lệ 1:2, có thể tạo 2 đồng phân: $1,2-\text{dinitroglycerin}$ và $1,3-\text{dinitroglycerin}$.
(4) Đúng. Trong phản ứng (1), nhóm $\text{-OH}$ của glycerol bị thay thế bằng $\text{-ONO}_2$.