Đề bài
Trong công nghiệp, ammonia được tổng hợp từ khí nitrogen và khí hydrogen theo phản ứng sau:
$\left. N_{2}{}_{(g)} + 3H_{2}{}_{(g)}~\rightleftarrows 2NH_{3}{}_{(g)} \right.$
Kết quả nghiên cứu sự phụ thuộc của hiệu suất phản ứng trên vào áp suất và nhiệt độ được thể hiện trong giản đồ sau:
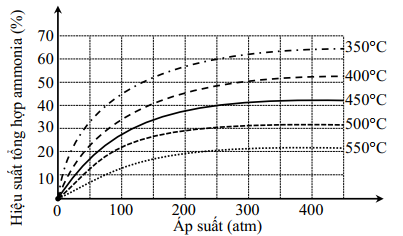
Ở nhiệt độ 450 $℃$, áp suất 250 atm, trộn 2 mol $N_{2}$ với 4,5 mol $H_{2}$ thu được bao nhiêu mol $NH_{3}$?
Phương pháp giải
Quan sát giản đồ, xác định hiệu suất phản ứng.
Viết PTHH, tính theo PTHH được số mol của $NH_{3}$.
Lời giải chi tiết
Theo giản đồ, ở nhiệt độ ${{450}^{o}}C$, áp suất 250 atm, hiệu suất phản ứng là 40%.
Ta thấy: ${{n}_{{{N}_{2}}}}=2$ > $\frac{{{n}_{{{H}_{2}}}}}{3}=\frac{4,5}{3}=1,5$
Do vậy phản ứng sẽ tính theo .
PTHH: $\left. N_{2}{}_{(g)} + 3H_{2}{}_{(g)}~\rightleftarrows 2NH_{3}{}_{(g)} \right.$
Theo PTHH, ${{n}_{N{{H}_{3}}}}=\frac{2}{3}.{{n}_{{{H}_{2}}}}.H=\frac{2}{3}.4,5.40\%=1,2(mol)$