Đề bài
Một học sinh tiến hành thí nghiệm để so sánh tính base trong dung dịch nước của một số amine và ammonia với dự đoán: “Khi số nguyên tử carbon trong phân tử amine tăng thì tính base của amine tăng, pH của dung dịch amin trong nước tăng”. Học sinh tiến hành như sau:
Chuẩn bị các cốc chứa dung dịch nồng độ 0,1M của các chất ở 25oC: NH3; CH3NH2; CH3CH2NH2; (CH3)2NH; CH3CH2CH2NH2.
Dùng máy đo pH để do giá trị pH của các dung dịch.
Đồ thị thể hiện kết quả thu được như sau:
So sánh pH của dung dịch 0.1 M các amine
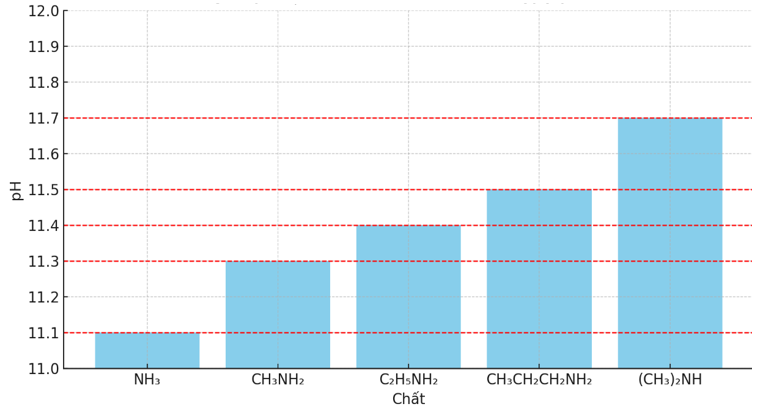
Phương pháp giải
Dựa vào pH của ${{C}_{2}}{{H}_{5}}N{{H}_{2}}$ ở 25°C, xác định được nồng độ của các ion.
Từ đó tính được giá trị Kb của phản ứng.
Quan sát biểu đồ để rút ra nhận xét về giả thuyết đưa ra.
Lời giải chi tiết
(a) Đúng vì: ${{C}_{2}}{{H}_{5}}N{{H}_{2}}$ có pH = 11,4 ở 25°C
Do đó, $\left[ {{C}_{2}}{{H}_{5}}N{{H}_{3}}^{+} \right] =\left[ O{{H}^{-}} \right]$= $10^{-14}/10^{-11,4}$$=$$2,512.10^{-3}$
$\Rightarrow [{{C}_{2}}{{H}_{5}}N{{H}_{2}}]=$ $0,1-{{2,512.10}^{-3}}=0,097488$
$\Rightarrow Kb=\frac{{{({{2,512.10}^{-3}})}^{2}}}{0,097488}={{6,5.10}^{-5}}$.
(b) Sai, ${{\left( C{{H}_{3}} \right)}_{2}}NH$có tên thường là dimethylamine.
(c) Sai, ta thấy ${{\left( C{{H}_{3}} \right)}_{2}}NH$ ít C hơn ${{C}_{2}}{{H}_{5}}C{{H}_{2}}N{{H}_{2}}$ nhưng ${{\left( C{{H}_{3}} \right)}_{2}}NH$ có pH cao hơn.
(d) Đúng, trong các chất khảo sát, $N{{H}_{3}}$ có pH nhỏ nhất nên tính base yếu nhất.