Đề bài
Cationite là một loại nhựa trao đổi cation được sử dụng để loại bỏ ion $Ca^{2 +},\ Mg^{2 +}$. Khi nước cứng đi qua cột nhựa, các ion $Ca^{2 +},\ Mg^{2 +}$(kí hiệu chung là M2+) sẽ được giữ lại và thay thế bằng các ion H+, Na+ theo sơ đồ sau: M2+ + 2 R-SO3X → (R-SO3)2M + 2 X+ (trong đó $X^{+}$ là $H^{+}$ hoặc $Na^{+}$)
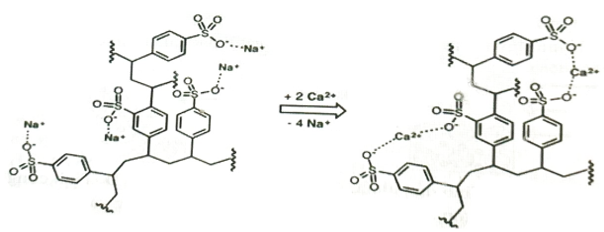
Một loại cationite có % khối lượng sulfur là 7,94% được sử dụng để loại bỏ các ion $Mg^{2 +},Ca^{2 +}$ trong nước cứng. Nếu một cột nhựa trao đổi ion trong thiết bị lọc nước gia đình có chứa 2,0 kg cationite trên thì tổng số mol $Mg^{2 +},Ca^{2 +}$ tối đa có thể được loại bỏ là bao nhiêu (làm tròn đến hàng phần trăm)?
Phương pháp giải
Tính khối lượng sulfur trong cationite.
Tính theo PTHH, tính được số mol $Mg^{2 +},Ca^{2 +}$.
Lời giải chi tiết
Khối lượng sulfur trong cationite là: ${{m}_{S}}=2.1000.7,94\%=158,8g$.
Số mol sulfur trong cationite là:${{n}_{S}}=\frac{158,8}{32}=4,9625mol$
Theo phương trình trao đổi:
$M^{2+} + 2 \text{ R-SO}_3X \rightarrow (\text{R-SO}_3)_2M + 2X^+$
Số mol $M^{2+}$ (tức tổng số mol $Mg^{2+}, Ca^{2+}$) tương ứng là: ${{n}_{{{M}^{2+}}}}=\frac{{{n}_{S}}}{2}=\frac{4,9625}{2}\approx 2,48\text{ mol}$
Vậy tổng số mol $Mg^{2+}, Ca^{2+}$ tối đa có thể được loại bỏ là 2,48 mol
Phương pháp giải
Dựa vào cơ chế trao đổi ion của cationite, đặc biệt là việc thay thế các ion $M^{2+}$ bằng $H^{+}, Na^{+}$.
Lời giải chi tiết
Bước 1: Tính khối lượng mol của nhóm R-SO3.
Khối lượng mol của S là 32 g/mol.
Theo bài, % khối lượng của sulfur là 7,94%, do đó:
$$\frac{m_{S}}{M_{R-SO_3}} = \frac{7,94}{100}$$
Đặt khối lượng mol của nhóm R-SO3X là M, ta có phương trình:
$$\frac{32}{M} = \frac{7,94}{100}$$
Giải phương trình ta tìm được:
$$M = \frac{32 \times 100}{7,94} \approx 403,28 \text{ g/mol}$$
Bước 2: Tính tổng số mol ion $Mg^{2+}, Ca^{2+}$ có thể loại bỏ:
Theo phương trình trao đổi:
$$M^{2+} + 2 \text{ R-SO}_3X \rightarrow (\text{R-SO}_3)_2M + 2X^+$$
Số mol nhóm R-SO3X trong 2 kg cationite là:
$$\frac{2000}{403,28} \approx 4,96 \text{ mol}$$
Số mol $M^{2+}$ (tức tổng số mol $Mg^{2+}, Ca^{2+}$) tương ứng là:
$$\frac{4,96}{2} \approx 2,48 \text{ mol}$$
Vậy tổng số mol $Mg^{2+}, Ca^{2+}$ tối đa có thể được loại bỏ là 2,48 mol (làm tròn đến hàng phần trăm là 2,5 mol).