Đề bài
Một pin điện hoá $\text{Zn} - \text{H}_{2}$ được thiết lập ở điều kiện thường như hình vẽ sau (vôn kế có điện trở rất lớn).
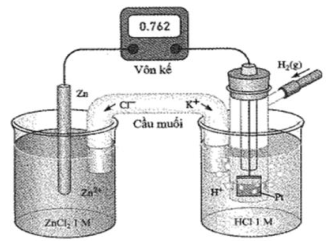
Phương pháp giải
Dựa vào sơ đồ pin điện hoá và lý thuyết về pin điện, điện phân.
Lời giải chi tiết
Phân tích các mệnh đề:
Mệnh đề 1: "Thế điện cực chuẩn của cặp oxi hoá - khử $\text{Zn}^{2 +}/\text{Zn}$ là $0,762~\text{V}$".
Sai, trong pin điện trên không được đặt trong điều kiện chuẩn.
Mệnh đề 2: "Chất điện li trong cầu muối là KCl.".
Đúng, chất điện li thường dùng trong cầu muối có thể là KCl, vì KCl là chất điện li phổ biến và trơ trong các phản ứng hóa học.
Mệnh đề 3: "Phản ứng hoá học xảy ra trong pin là: \(\text{Zn}(\text{s}) + 2\text{H}^{+}(\text{aq})\rightarrow\text{Zn}^{2 +}(\text{aq}) + \text{H}_{2}(\text{g})\)."
Đúng, đây chính là phản ứng xảy ra khi pin hoạt động, trong đó kẽm bị oxi hóa và ion H+ bị khử để tạo thành H2.
Mệnh đề 4: "Quá trình khử xảy ra ở cathode là: \(2\text{H}^{+} + 2\text{e}\rightarrow\text{H}_{2}\)."
Đúng, Ở cathode, quá trình khử H+ để tạo thành H2 diễn ra.